
STF: 2ª Turma decide hoje sobre possível liberação da prisão preventiva de Daniel Vorcaro
Em sessão virtual iniciada em 13/03/2026, colegiado avalia se referenda ou revisa decisão individual do ministro André Mendonça no caso ligado ao Banco Master
A patente da semaglutida, substância presente em medicamentos como Ozempic, Wegovy e Rybelsus, tem validade até 20 de março de 2026 no Brasil. A partir dessa data, outras farmacêuticas poderão pedir registro para produzir versões genéricas ou similares do composto no país, desde que obtenham autorização da Anvisa. O princípio ativo é amplamente utilizado no tratamento de diabetes e obesidade e, com o fim da exclusividade, cresce a expectativa de ampliação da oferta no mercado farmacêutico nacional.
O término da proteção, no entanto, não significa que os genéricos estarão disponíveis imediatamente nas prateleiras. Qualquer novo produto à base de semaglutida ainda terá de cumprir todas as etapas de registro e avaliação regulatória antes de chegar às farmácias.
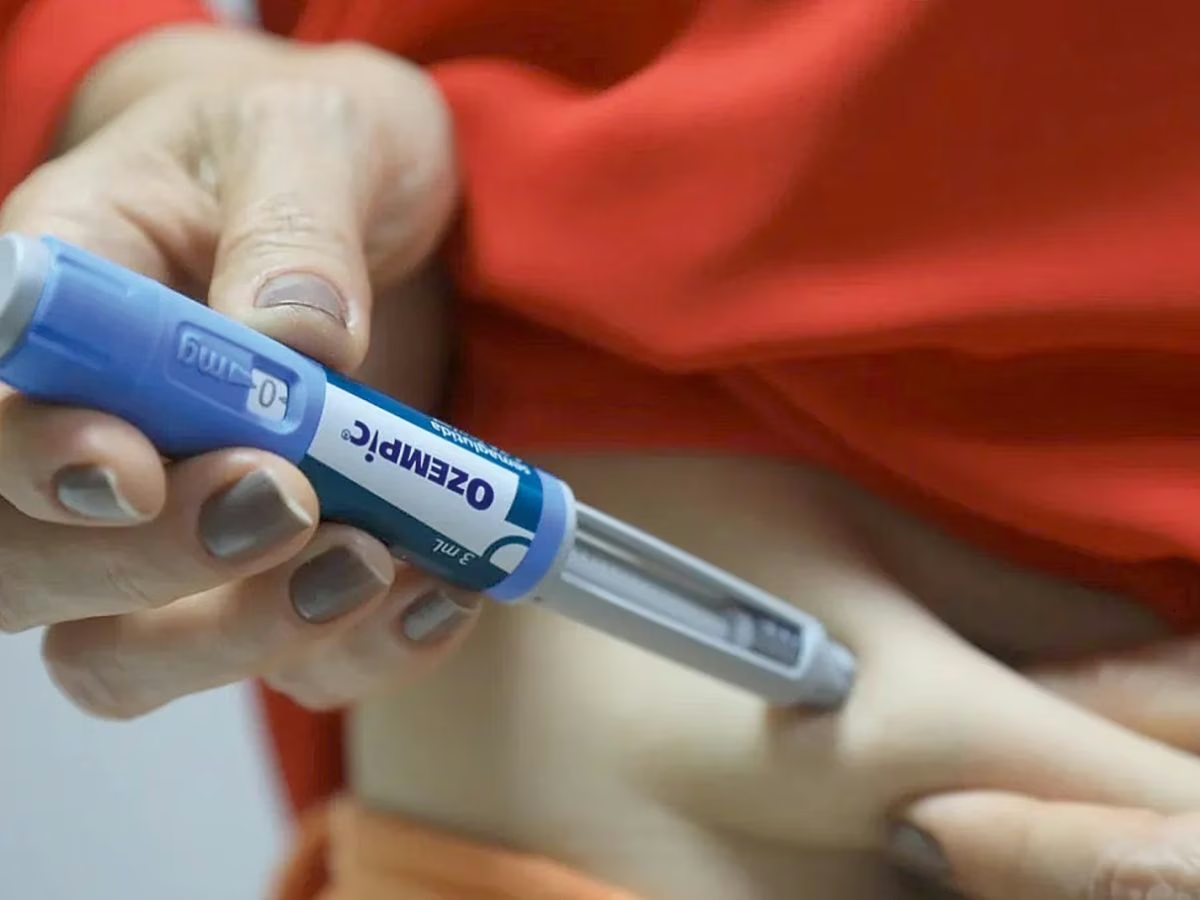
Ozempic
Foto: Divulgação
A discussão sobre a possível prorrogação de patentes ligadas a produtos da Novo Nordisk chegou ao Superior Tribunal de Justiça (STJ). Em decisão divulgada em 12 de janeiro de 2026, a Quarta Turma do tribunal reforçou que o prazo de patente de invenção é de 20 anos a partir do depósito e não pode ser estendido judicialmente em razão de eventual demora do Instituto Nacional da Propriedade Industrial (INPI).
Na prática, isso significa que a proteção vinculada à semaglutida se encerra em 20 de março de 2026, abrindo caminho para que concorrentes tentem registrar seus próprios medicamentos com a mesma substância, desde que atendam às exigências técnicas e regulatórias brasileiras.
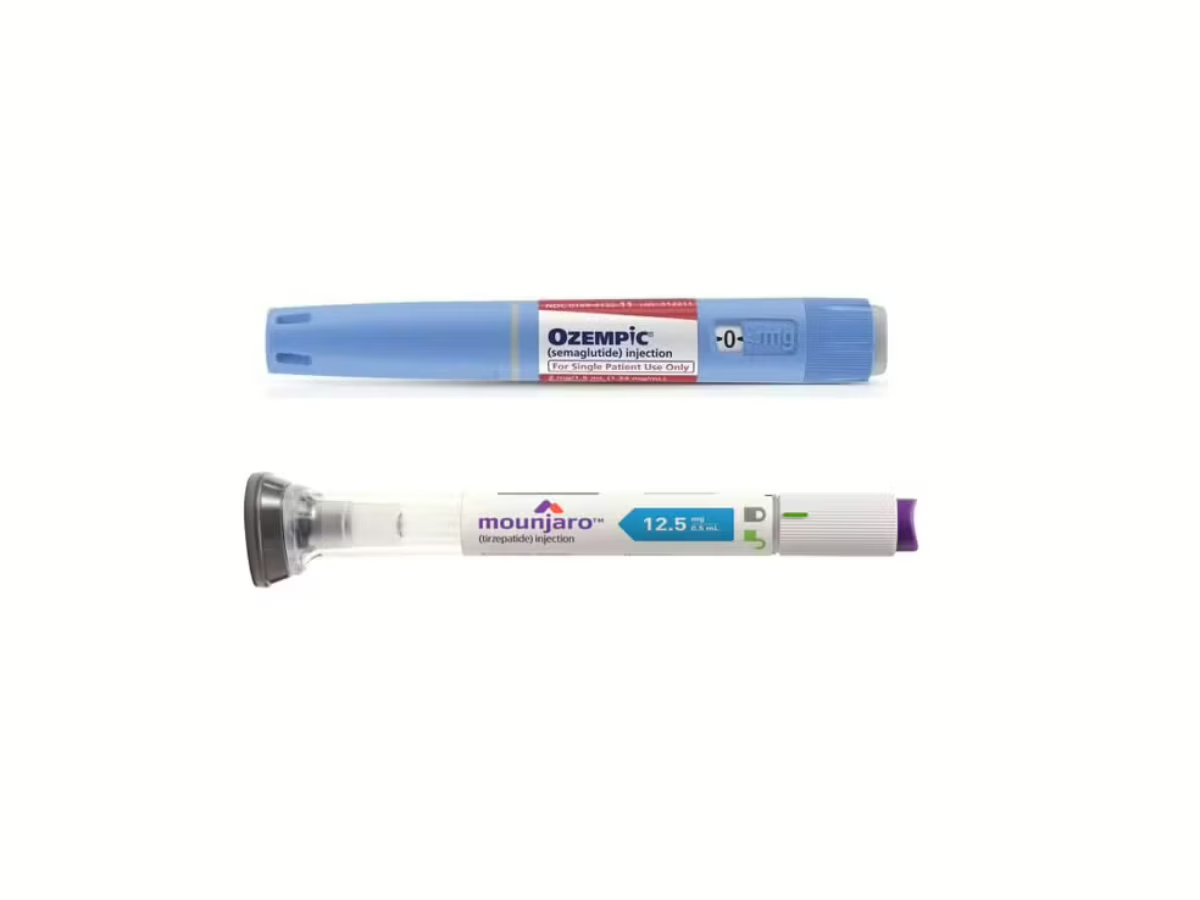
Canetas Ozempic e Mounjaro
Foto: Reprodução/Novo Nordisk e Eli Lilly
No campo regulatório, a Anvisa informou que dará prioridade à análise de processos de registro relacionados à semaglutida e à liraglutida. Segundo a agência, a medida atende a pedido do Ministério da Saúde e está ligada a objetivos de fortalecer a fabricação nacional no âmbito do Complexo Econômico-Industrial da Saúde.
Com isso, empresas interessadas em lançar versões genéricas ou similares ganham um ambiente regulatório mais favorável em termos de celeridade de análise. Ainda assim, o tempo até que novos produtos cheguem às farmácias dependerá da qualidade dos dossiês apresentados, da capacidade produtiva e do cumprimento dos requisitos sanitários.
Para pessoas em tratamento de diabetes e obesidade, a expectativa é de que o aumento da concorrência provoque uma pressão gradual por redução de preços. Esse movimento, porém, tende a ser progressivo e condicionado à quantidade de fabricantes, às estratégias comerciais e ao ritmo de aprovação dos novos registros. Não há mudança automática nos valores a partir de 20 de março de 2026.
No Sistema Único de Saúde (SUS), o debate sobre a incorporação desses medicamentos ganha novo fôlego justamente por causa do custo. Em agosto de 2025, a Comissão Nacional de Incorporação de Tecnologias no SUS (Conitec) recomendou não incorporar liraglutida e semaglutida à rede pública. Na época, foi estimado um impacto financeiro em torno de R$ 8 bilhões anuais, valor considerado um dos principais entraves.
Uma eventual queda de preços, impulsionada pela entrada de genéricos e similares, pode influenciar futuras reavaliações da Conitec. Ainda assim, o fim da patente e a possível redução de custos não alteram de imediato a decisão anterior de não incorporar essas tecnologias.
No Brasil, medicamentos inovadores podem ter patente por até 20 anos, período em que a empresa responsável pela invenção mantém o direito exclusivo de produção e comercialização, como forma de compensar investimentos em pesquisa e desenvolvimento. Encerrado esse prazo, outras companhias passam a poder fabricar versões equivalentes, que precisam ser avaliadas e aprovadas pela Anvisa antes de serem ofertadas.
Pelas regras brasileiras, remédios genéricos — comercializados apenas pelo nome da substância — devem custar pelo menos 35% menos que o medicamento de referência. Um levantamento conduzido por pesquisadores da Universidade de Brasília e da Universidade Federal de Santa Catarina mostrou que, na prática, a diferença tende a ser ainda maior: em média, genéricos chegam a ser 59% mais baratos que os produtos de marca, enquanto os similares têm preços cerca de 15% menores.
Esses parâmetros ajudam a explicar por que o fim da exclusividade da semaglutida é visto como um potencial divisor de águas para o acesso a tratamentos para obesidade e diabetes no país.
Para farmácias e profissionais de saúde, a proximidade do fim da patente deve aumentar a demanda por informação sobre “genéricos” e “similares” de semaglutida. Especialistas reforçam que somente produtos com registro válido na Anvisa oferecem as garantias de qualidade, segurança e eficácia exigidas pela legislação sanitária.
Promessas de “semaglutida mais barata” fora do circuito regulado exigem cautela, especialmente diante da alta procura por medicamentos emagrecedores e para controle glicêmico. Enquanto isso, empresas interessadas podem avançar com suas estratégias e pedidos de registro, e órgãos públicos devem seguir monitorando o cenário de preços para eventuais revisões de políticas no SUS.
Os próximos meses serão decisivos para definir quantos fabricantes efetivamente conseguirão ingressar no mercado e em que ritmo os efeitos do fim da patente da semaglutida serão sentidos no bolso dos pacientes e nas contas públicas.















